

科学家们已经能在实验室利用细胞培育、分化、自组装成各种类似人体组织的 3D 结构,制造出肝脏、胰脏、胃、心脏、肾脏甚至乳腺等在内的各种类器官。
今日我们看到日本的权威报道!东京医科齿科大学研究成果!成功培育出了肝脏、胆管、胰脏,今天小编为带大家播报这一突破性新闻。
研究要点
●研究小组利用人类iPS细胞成功培育出了肝胆胰腺发生的类器官模型。
●发现了肝脏-胆管等脏器之间的连结与发展高效率的再生医疗技术息息相关。
●从单一器官再生,到多器官统一培育,基于全新理念的器官培养技术有望在今后得以推广。
通过模仿子宫中的肝,胆和胰腺等生长的过程,研究小组开发了一种世界领先的技术,可以利用人类iPS细胞生成肝、胆、胰连接在一起的微型多器官。此外,还在试管中成功再现了多脏器生长时发生异变引起遗传疾病的过程。培养出的微型多器官已确认具有分泌胆汁功能。目前正进行进一步研究,有望应用于治疗性移植。这项研究的结果于2019年9月25日下午6点(英国时间)发表在国际科学杂志《自然》的网络版上。

项目负责人 武部 貴則 教授
研究背景
人的身体是从一个受精卵开始渐渐长成的,经过数百数千甚至数十兆细胞的分化,形成各种各样的器官,和个体本身。近年来,通过在试管内模仿其发生学过程,从人类IPS细胞等尚未成熟的干细胞中人工培育特定器官的尝试备受关注。
但是,通过只诱导特定脏器(单一脏器)的传统模式,相邻的多个脏器之间的连接无法完全吻合。因此存在着培育出的脏器不能充分发挥功能,或者不能持久使用等重大未解决问题。例如,与肝脏相邻的脏器“胆管”狭窄导致胆道闭锁症等疾病,会缓慢伤害肝脏,最终导致肝衰竭。
因此,研究小组认为,为了实现再生医疗的终极目标-----将丧失的功能完全恢复(再生),有必要从根本上重新考虑脏器的设计思想(范式转移)。也就是说,考虑到与周边器官的连接性,开发复杂的多器官创生技术是当务之急。在这次的研究中,研究小组着眼于研究在子宫内各器官之间如何连结,并通过在试管中人为地情景再现,研发出世界首个人类IPS细胞培育的微型多器官,并为今后该课题的进一步发展打下了坚实的基础。
研究成果概要
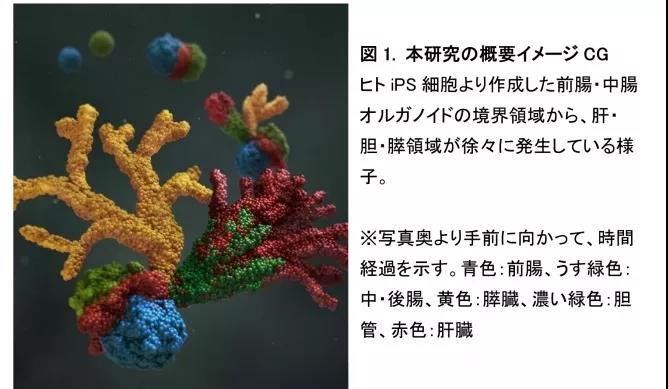
已知肝胆胰器官结构域是从受精后8周左右形成的前驱组织的边界领域发展而来的,该区域被称为前肠球体和中肠球体。因此,本研究着眼于发育初级阶段所存在的前肠球体·中肠球体之间的边界相互作用,并试图对它们进行再现(图1)。首先,利用人类IPS细胞分别诱导出前肠、中肠组织(图2a)。接下来,将它们连接起来,制成前肠-中肠边界(边界层)。令人惊讶的是,我们发现肝脏、胆管和胰脏的前驱细胞是从边界区域自发诱导的 (图2b)。
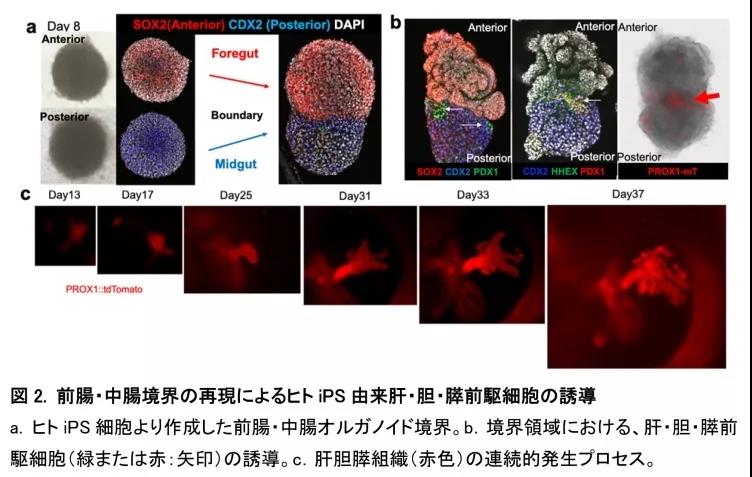
从人类多能干细胞分化而来的前肠球体和后肠球体之间的边界相互作用使得视黄酸依赖的肝胆胰脏器官结构域在前肠-中肠边界类动物体中存在,而不需要外在因素。移植物衍生的组织以中肠衍生物为主,长期培养的显微解剖的肝胆胰类器官发育成分离的多器官类似物,并概括了早期形态发生事件,包括三个不同且相互连接的器官结构的内陷和分支,使人联想起源自小鼠的前肠中肠培养物。如在体内观察到的,HES1基因突变引起的多器官结构域的错误分离消除了胆汁特异性培养的潜力。
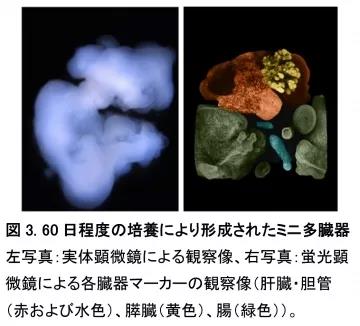
总而言之,研究人员证明可以通过并列前肠和中肠组织建立实验性多器官整合模型,并可能作为研究复杂的人类内胚层器官发生的易处理、可操纵和易获取的模型。
据了解,器官发生是一个复杂且相互联系的过程,由多个边界组织相互作用而实现。但是,尚不清楚各个相邻的部分如何协调以建立一个完整的多器官结构。
研究成果的意义
摆脱了传统单一器官再生概念,转变为基于周边组织连结的多器官一次性创生(系统再生),对今后的器官培养方向产生了巨大影响,成功为肝胆胰组织一次性创生技术打下了基础,一定程度上推动了人类生物学研究的进展,成为解析胎内复杂人体器官形成的有效工具,此前人类一直难以解析。
此外,还可以水平扩展到各种器官(例如,肾系统(血管-肾脏-输尿管/膀胱)和肺系统(气管-肺泡-毛细血管)以及中枢神经系统(脑脊髓 末梢神经/组织)等等)。将来,如果能够建立基于“多器官(系统)创生”这一创新概念的移植技术,可以预见,它将不仅可以拯救众多等待器官移植的患者,也能给再生医疗做出巨大的贡献。
